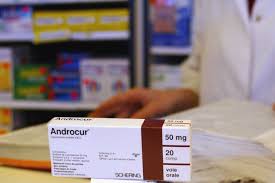
Rappelons que l’alerte est donnée depuis 2008 par le Professeur FROELICH, Chef du service de neurochirurgie de l'Hôpital Lariboisière (Paris), qui a publié son étude démontrant le lien entre la prise prolongée d’ANDROCUR et le risque important d’apparition de méningiomes.
Rappelons également le silence inquiétant des autorités de 2008 à octobre 2018 date à laquelle l’ANSM commencera à communiquer sur le risque pourtant connu depuis … 10 ans ! Dix longues années au cours desquelles les malades ont consommé un médicament en confiance alors que les autorités sanitaires et le laboratoire en connaissaient la dangerosité.
Rappelons pour finir que, depuis octobre 2018, on tourne autour du pot : les mesures annoncées dans le communiqué de l’ANSM du 12 juin 2019 se bornant à entériner ce qui avait déjà été discuté depuis octobre 2018, c’est-à-dire informer correctement sur le risque.
Les mesures prises par l’ANSM n’ont donc rien d’extraordinaire sauf le retard (fautif ?) avec lequel elles interviennent.
C’est exactement ce que reproche notre cliente, Madame X, victime de multiples méningiomes diagnostiqués et opérés en 2013. C’est à son arrivée aux Urgences à Poitiers, alors qu’elle perdait la vue, que les médecins l’informent de la nécessité d’arrêter immédiatement le traitement.
Elle sera opérée des méningiomes les plus accessibles. Pour les autres, il faut vivre avec tout en subissant les effets secondaires particulièrement invalidant (fatigue chronique, trouble de la concentration ayant imposé un aménagement de son contrat de travail, allodynie, hyperesthésie, paresthésie avec point gâchette, troubles visuels, anosmie …).
Auparavant, et alors qu’elle est traitée par ANDROCUR de manière continue depuis 1995, ni ses médecins, ni son pharmacien, ni le laboratoire, ni les autorités n’ont informé Madame X du risque important et pourtant connu de la communauté médicale et des autorités. Aucun suivi particulier ne lui a été recommandé. On peut se demander si nous n’avons pas à faire à une conjuration des imbéciles … ou des lâches. Car bien évidemment, les différents protagonistes vont adopter la défense du « ce n’est pas moi c’est lui ».
On peut aisément comprendre la colère de Madame X qui aurait dû recevoir l’information dès 2008, ce qui lui aurait permis d’être suivie, ou même d’arrêter son traitement et d’éviter une lourde opération en 2013.
Depuis 2008, l’étude initiale du Professeur FROELICH n’a jamais été remise en question. Au contraire.
Fallait-il attendre plus de 10 années avant de réagir ? Ne fallait-il pas ne serait-ce que par précaution, informer les professionnels de santé et les patients dès 2008 ? Certainement.
En tout état de cause rien ne l’empêchait et le risque était suffisamment connu et les conséquences suffisamment graves pour justifier la délivrance d’une information ciblée aux médecins et aux patients concernées.
Les médicaments sont des produits considérés comme assez dangereux pour justifier l’existence d’une autorité, prétendument indépendante, en charge de la pharmacovigilance et de la protection des patients. Et l’ANSM créée en 2012, avait succédé à l’Afssaps qui avait démontré son inefficacité et ses insuffisances, notamment dans le dossier MEDIATOR.
C’est cette autorité – source théorique de la confiance des malades – qui devait au besoin contraindre le laboratoire à délivrer une information pertinente tout en s’assurant des moyens mis en œuvre pour que cette information soit bien reçue. Ce n’est pas en ajoutant une mention de quelques lignes dans la notice d’un médicament qu’on ne lit plus forcément après des années de traitement qu’on peut estimer avoir délivré une information pertinente, efficace et suffisante.
Une mention d’alerte claire sur l’emballage pendant quelques mois aurait tout simplement pu permettre à certaines femmes de ne pas subir les préjudices auxquelles elles sont contraintes de faire face aujourd’hui : combien d’opérations au cerveau aurait-on pu éviter ? combien d’heures d’angoisse ont-elles été supportées par les malades désinformées et maltraitées ?
Rappelons également le silence inquiétant des autorités de 2008 à octobre 2018 date à laquelle l’ANSM commencera à communiquer sur le risque pourtant connu depuis … 10 ans ! Dix longues années au cours desquelles les malades ont consommé un médicament en confiance alors que les autorités sanitaires et le laboratoire en connaissaient la dangerosité.
Rappelons pour finir que, depuis octobre 2018, on tourne autour du pot : les mesures annoncées dans le communiqué de l’ANSM du 12 juin 2019 se bornant à entériner ce qui avait déjà été discuté depuis octobre 2018, c’est-à-dire informer correctement sur le risque.
Les mesures prises par l’ANSM n’ont donc rien d’extraordinaire sauf le retard (fautif ?) avec lequel elles interviennent.
C’est exactement ce que reproche notre cliente, Madame X, victime de multiples méningiomes diagnostiqués et opérés en 2013. C’est à son arrivée aux Urgences à Poitiers, alors qu’elle perdait la vue, que les médecins l’informent de la nécessité d’arrêter immédiatement le traitement.
Elle sera opérée des méningiomes les plus accessibles. Pour les autres, il faut vivre avec tout en subissant les effets secondaires particulièrement invalidant (fatigue chronique, trouble de la concentration ayant imposé un aménagement de son contrat de travail, allodynie, hyperesthésie, paresthésie avec point gâchette, troubles visuels, anosmie …).
Auparavant, et alors qu’elle est traitée par ANDROCUR de manière continue depuis 1995, ni ses médecins, ni son pharmacien, ni le laboratoire, ni les autorités n’ont informé Madame X du risque important et pourtant connu de la communauté médicale et des autorités. Aucun suivi particulier ne lui a été recommandé. On peut se demander si nous n’avons pas à faire à une conjuration des imbéciles … ou des lâches. Car bien évidemment, les différents protagonistes vont adopter la défense du « ce n’est pas moi c’est lui ».
On peut aisément comprendre la colère de Madame X qui aurait dû recevoir l’information dès 2008, ce qui lui aurait permis d’être suivie, ou même d’arrêter son traitement et d’éviter une lourde opération en 2013.
Depuis 2008, l’étude initiale du Professeur FROELICH n’a jamais été remise en question. Au contraire.
Fallait-il attendre plus de 10 années avant de réagir ? Ne fallait-il pas ne serait-ce que par précaution, informer les professionnels de santé et les patients dès 2008 ? Certainement.
En tout état de cause rien ne l’empêchait et le risque était suffisamment connu et les conséquences suffisamment graves pour justifier la délivrance d’une information ciblée aux médecins et aux patients concernées.
Les médicaments sont des produits considérés comme assez dangereux pour justifier l’existence d’une autorité, prétendument indépendante, en charge de la pharmacovigilance et de la protection des patients. Et l’ANSM créée en 2012, avait succédé à l’Afssaps qui avait démontré son inefficacité et ses insuffisances, notamment dans le dossier MEDIATOR.
C’est cette autorité – source théorique de la confiance des malades – qui devait au besoin contraindre le laboratoire à délivrer une information pertinente tout en s’assurant des moyens mis en œuvre pour que cette information soit bien reçue. Ce n’est pas en ajoutant une mention de quelques lignes dans la notice d’un médicament qu’on ne lit plus forcément après des années de traitement qu’on peut estimer avoir délivré une information pertinente, efficace et suffisante.
Une mention d’alerte claire sur l’emballage pendant quelques mois aurait tout simplement pu permettre à certaines femmes de ne pas subir les préjudices auxquelles elles sont contraintes de faire face aujourd’hui : combien d’opérations au cerveau aurait-on pu éviter ? combien d’heures d’angoisse ont-elles été supportées par les malades désinformées et maltraitées ?
Dans le dossier ANDROCUR, on constatera que pendant 10 années ni les autorités, ni le laboratoire, ni les médecins, ni les pharmaciens ne délivreront d’information particulière, ce qui témoigne d’un indécrottable défaut d’information ! Pour protéger quels intérêts ? la santé ou la rentabilité de Bayer ?
Pourtant, les mesures de bon sens n’étaient pas compliquées à trouver, elles étaient simples, peu couteuses. Même la sécurité sociale y aurait trouvé son compte en ne prenant pas en charge de dispendieuses opérations complexes nécessitant plusieurs jours d’hospitalisation.
Pourtant, les mesures de bon sens n’étaient pas compliquées à trouver, elles étaient simples, peu couteuses. Même la sécurité sociale y aurait trouvé son compte en ne prenant pas en charge de dispendieuses opérations complexes nécessitant plusieurs jours d’hospitalisation.
Aujourd’hui, après le MEDIATOR, la DEPAKINE, ESSURE, le LEVOTHYROX (pour ne citer que les principaux), les patients ne peuvent ni admettre ni comprendre le mépris dont font preuve les autorités de santé et les financiers de la chimie. Les professionnels connaissaient les risques depuis dix ans et personne n’a alerté chaque malade. Faut il rappeler le principe énoncé par Hippocrate : primum non nocere. Un médicament doit soigner, et non rendre encore plus malade.
Madame X considère à l’évidence que l’autorité et l’institution médicale ont failli à son égard. C’est la raison pour laquelle elle m’a confié son dossier.
En effet, les personnes victimes de méningiomes diagnostiqués à partir de 2008 peuvent légitimement reprocher l’abstention fautive dans la délivrance d’une information importante ayant au moins privé le patient de faire le choix de poursuivre sous surveillance ou d’interrompre leur traitement.
Je ne manquerai pas de revenir vers vous dès que les premiers résultats judiciaires seront connus.
Romain Sintès
Avocat au barreau de Toulouse
Aux côtés de son associé, Christophe Lèguevaques,
il intervient dans de nombreux dossiers médicaux
ou d’action collective conjointe.
Avocat au barreau de Toulouse
Aux côtés de son associé, Christophe Lèguevaques,
il intervient dans de nombreux dossiers médicaux
ou d’action collective conjointe.


 Un avocat ?
Un avocat ?